大家好,我是青医14级石晓梦,目前肾内科师资博士后,借此分享一些基础实验心得。对于还未接触过基础实验的低年级同学而言,明确实验目的后,开始做一项实验之前,需要整理出该项实验的基本原理,具体操作步骤及注意事项,提前准备好所需试剂、材料及设备等。实验试剂的选择决定具体操作步骤,仔细研读试剂说明书及既往发表论文的实验过程,尽可能细化实验步骤尤为重要。初次尝试时最好有人帮带,如果是全新领域实验,遇到问题可以咨询试剂厂家,调整实验体系。基础实验要做好试错的准备。一定要注意实验安全问题,做好防护是重中之重!
这次具体分享的一个实验操作技能是瞬时转染,它就像是我们研究细胞、探索基因功能以及生产蛋白质药物的一把“金钥匙”。
一、概念
瞬时转染(transient transfection)是指将外源核酸(主要为质粒DNA、mRNA或小干扰RNA)通过物理或化学方法导入真核细胞,使其在限定时间内实现外源基因的短期表达。外源核酸不整合至宿主细胞基因组,随着细胞分裂逐渐被稀释,表达水平通常在转染后24–96小时达到峰值,随后迅速衰减。
与稳定转染(stable transfection)不同,瞬时转染无需抗性筛选,周期短(2–5天),适用于基因功能快速分析、蛋白质瞬时表达及病毒载体包装等场景。
二、主要用途
基因功能研究:通过过表达或RNA干扰(RNAi)等手段,观察目标基因对细胞表型(增殖、凋亡、信号通路等)的影响。
重组蛋白快速制备:在哺乳动物细胞中实现翻译后修饰完整的重组蛋白、抗体或酶的小规模表达,用于结构分析、活性检测等。
病毒载体包装:将包装质粒与目的质粒共转染至包装细胞系(如HEK293T),瞬时产生高滴度慢病毒、腺病毒或腺相关病毒颗粒。
药物靶点验证:在细胞模型中瞬时表达潜在药物靶点,用于化合物筛选或靶点功能验证。
三、操作步骤:一场精心设计的“细胞快递”
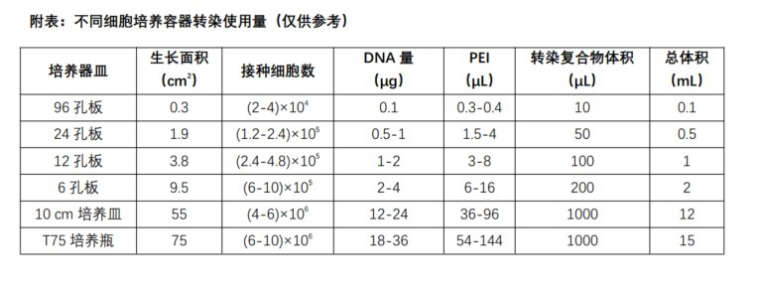
具体反应体系参考转染试剂说明书(见下文附图),以下是为了便于理解该实验过程。
整个瞬时转染过程,就像一次精密的分子生物学实验,主要分为三大步:
第一步:准备“货物”与“收件人”
货物(质粒DNA):首先,我们要构建一个含有目标基因的环状DNA分子——质粒。这个质粒必须经过高纯度提取,不能含有细菌内毒素等污染物,否则会“毒害”细胞。
收件人(细胞):我们需要状态良好的细胞。通常,在转染前一天,我们会将细胞接种到培养皿中,确保转染当天细胞处于对数生长期,且融合度(细胞覆盖培养皿底部的面积比例)在70%-90%之间。细胞状态是转染成功的关键!
第二步:选择“快递员”(转染试剂)
DNA本身带负电,而细胞膜也带负电,同性相斥,DNA自己进不去。所以我们需要“快递员”来帮忙。最常用的快递员是阳离子脂质体(如Lipo2000、Lipo3000、Fugene等)。它们就像微小的“泡泡”,带正电,可以包裹住带负电的DNA,形成“脂质体-DNA复合物”。这个复合物更容易被细胞膜“接纳”,通过内吞作用进入细胞。
操作:通常在一个离心管里,将转染试剂和DNA按比例分别稀释在无血清的培养基中,然后轻轻混合,室温孵育15-20分钟,让复合物充分形成。
第三步:“送货上门”(转染过程)
将孵育好的“脂质体-DNA复合物”直接、均匀地滴加到培养好的细胞中。
轻轻摇晃培养皿,使其混合均匀。
将细胞放回培养箱(37℃,5% CO₂)中继续培养。
然后,就是等待:
4-6小时后,可以更换新鲜的完全培养基,以降低转染试剂的毒性。
24-48小时后,是检测基因表达(比如用荧光显微镜观察报告基因GFP)的黄金时间。
48-72小时后,通常是收集细胞裂解液或培养上清,检测目标蛋白产量的高峰期。
四、关键注意事项
1.细胞状态
细胞代数宜控制在20代以内,融合度过高或过低均显著影响转染效率。支原体污染可导致转染效率下降50%以上,需定期检测。
2.核酸质量
质粒DNA纯度要求A₂₆₀/₂₈₀介于1.7–1.9,内毒素水平应低于0.1 EU/μg。内毒素可激活细胞免疫应答,降低转染效率并诱导细胞凋亡。
3.转染条件优化
不同细胞类型对转染试剂的敏感性差异显著。需针对具体细胞系优化关键参数:
核酸与转染试剂的质量比
单位面积核酸用量
以转染效率与细胞存活率的平衡为评价指标。
4.无菌与生物安全
全程须在生物安全柜中无菌操作。涉及病毒包装、致癌基因或基因编辑时,应依据风险等级在相应生物安全级别(BSL-2及以上)实验室中开展。
5.血清影响
阳离子脂质体类试剂在复合物形成阶段应避免血清存在;转染后及时补充血清以维持细胞活性。

以上是对瞬时转染的分享。在分子生物学实验方面,我有一些经验,如果有其他基础实验问题,欢迎一起交流。我的微信:alleysxm